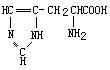
组氨酸
英文名称:histidine
英文缩写:His
CAS号:(71-00-1)
组氨酸在1896年由德国物理学家艾布瑞契.科塞尔|艾布瑞契•科塞尔首次分离出来。
性质
α-氨基β-咪唑基丙酸,属于碱性氨基酸或杂环氨基酸。由Pa-uli反应即和重氮苯磺酸反应产生红色。有D,D,L-及混旋体(L为拉丁文左的意思,D是拉丁文DEXTRO,右的意思,D,L指的是氨基酸分子结构的手性)存在于珠蛋白内。也是存在肌肉中的一种肌肽成分。L-组氨酸无色片状或针状结晶,无臭,稍有苦味。227℃软化,277℃分解。溶于水。旋光度 -39.4°(c=1.13,水中)。以干面粉,猪、牛血粉,猪毛或蹄甲为原料制取,也可由葡萄糖发酵制得。组氨酸与其他氨基酸相比,除一些常见的化学反应外,由于其右侧链咪唑基与重氮苯磺酸能形成棕红色化合物,即波利(Pauly)反应。由于咪唑基解离常数为6.0,即解离的质子浓度与水的相近,因此组氨酸既可作为质子供体,又可作为质子受体。另一方面,咪唑基供出质子和接受质子的速度十分快,半寿期小于10-10s,且供出质子和接受质子的速度几乎相等。组氨酸残基在活性蛋白中常为活性中心。组氨酸为半必需氨基酸,可作为药物或生化试剂。对人体来说,组氨酸可由普通的中间代谢产物合,因此一直被认为是非必需氨基酸,但随研究的深入,人们发现幼龄动物和婴儿体内的组氨酸合成量不能满足机体生长需要,即使是成年动物,若不从食物中补充,体内合成的也不能满足需要,所以人们又称之为半必需氨基酸。
组氨酸还是一些医药中间体合成的必备原材料之一,比如蓝铜胜肽ghk-cu.
现在已经知道,在生物体内的主要代谢途径有通过组氨酸脱氨酶进行脱氨,通过脱羧酶形成组胺以及氨基转移反应。生物合成是从ATP的腺嘌呤部分和磷酸核糖丝磷酸形成咪唑甘油磷酸,进行氨基转换反应。
L-组氨酸是一种半必需氨基酸,对于婴幼儿及动物的成长尤其重要。可作为生化试剂和药剂,还可用于治疗心脏病,贫血,风湿性关节炎等的药物。组氨酸存在于香蕉,葡萄,肉类,禽畜,牛奶以及奶类制品中。此外,组氨酸也存在于绿色蔬菜中,不过含量较少。
胃肠解痉药
名称(英) Histidine 组氨酸
用量用法 皮注或肌注:每次%溶液5ml。
组氨酸生产工艺
一, 一次浓缩段
原料:一次母液(胱氨酸生产中一次中和段产物)
辅料:蒸汽
将一次母液通入一次浓缩罐内,通入蒸汽,温度120,气压-0.09 Mpa,浓缩时间6h,结晶,过滤。
终点产物:结晶液(一次脱色段)结晶体,(NH4CL)回收利用
二, 一次脱色段
辅料:活性炭,纯水
结晶液进入一次脱色罐,投(通)入活性炭,纯水,温度70,脱色时间2h,过滤
终点产物:1,滤渣(回收利用)2,溶液(去上柱段)
三, 上柱段
辅料:阳离子交换树脂,纯水,0.1mol/L氨水
溶液进入阳离子交换柱内(流速500L/h),上柱量:100kg/2柱,上柱毕,定量水洗,纯水用量是柱体积的一倍,水洗过后溶液用0.1mol/L氨水洗脱并收集至第二柱流出液有组氨酸的Pauly反应时止.
终点产物:组氨酸收集液(去浓缩赶氨段)
四, 浓缩赶氨段
辅料:纯水
组氨酸收集液勇高效薄膜浓缩到粘稠状,加纯水适当稀释,出料,
终点产物:浓缩稀释液(去脱色段)
五, 脱色段
辅料:6mol/L的HCL
浓缩稀释液勇6mol/L HCL调PH7.5,加活性炭脱色,板框压滤,滤液用泵泵入浓缩锅
终点产物:1,脱色滤液(去浓缩结晶段)
六, 浓缩结晶段
浓缩液在浓缩锅,在80-90度下,真空浓缩到有大量结晶出现,放料,冷析,离心收集组氨酸,即得组氨酸的粗品,母液回收,再利用。
七, 精制段
组氨酸粗品加水,升温到70度,校正Ph值,加活性炭脱色,保温搅拌1H,脱色的透光率要达到99%以上,板框过滤,滤液经超滤后,用泵泵入浓缩锅,在高真空,80-90度以下,浓缩到有大量结晶出现,放料,冷析,离心收集组氨酸,即得组氨酸精品,母液回收,再利用。
组氨酸精品置于双锥旋转蒸发干燥器内干燥到水分达标
终点产物:L-组氨酸成品