滴定
滴定是一种化学实验操作也是一种定量分析的手段。它通过两种溶液的定量反应来确定某种溶质的含量。滴定最基本的公式为:
c1 V1 / ν1 = c2 V2 / ν2
其中c为溶液浓度,V为溶液体积,ν为反应方程序中的系数。
原理
滴定过程需要一个定量进行的反应,此反应必须能完全进行,且速率要快,也就是平衡常数、速率常数都要较大。而且反应还不能有干扰测量的副产物,副反应更是不容许的。
在两种溶液的滴定中,已知浓度的溶液装在滴定管里,未知浓度的溶液装在下方的锥形瓶里。通常把已知浓度的溶液叫做标准溶液,它的浓度是与不易变质的固体基准试剂滴定而测得的。
反应停止时,读出用去滴定管中溶液的体积,即可用公式算出浓度。
根据反应类型的不同,滴定分为以下种类:
酸碱中和滴定(利用中和反应) (指示剂常用甲基橙、酚酞、石蕊)
氧化还原滴定(利用氧化还原反应)
沉淀滴定(利用生成沉淀的反应)
络合滴定(利用络合反应)
指示剂
滴定反应需要灵敏的指示剂来指示反应的完成。指示剂在反应完成时,会迅速变成另一种颜色。这样实验者就可以根据指示剂的变色来确定反应的终止。
中和滴定的指示剂是有机弱酸或弱碱,它们的变色范围在等电点附近。如弱酸的变色(以HIn代表):
HIn (酸色形) = H+ + In-(碱色形)
指示剂一般有两种形态,两种形态呈现不同的颜色。指示剂在变色范围内呈现过渡色。有的指示剂有三种不同颜色的形态。
由于在变色范围时会发生“突跃”现象,颜色会变得很迅速,只要1滴溶液就可以让指示剂完全变色,因此选择指示剂时,只需让反应完成时的pH值落在突跃范围内即可,不必苛求准确。
其他种类滴定的指示剂一般是与某种反应物有灵敏反应的物质。当反应物消耗完毕时,指示剂就会变色。甚至有些反应物也可以作为指示剂,如高锰酸钾
操作
进行滴定时,应将滴定管垂直地夹在滴定管架上。
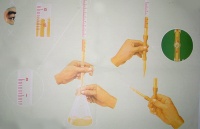
如使用的是酸管,左手无名指和小手指向手心弯曲,轻轻地贴着出口管,用其余三指控制活塞的转动。但应注意不要向外拉活塞以免推出活塞造成漏水;也不要过分往里扣,以免造成活塞转动困难,不能操作自如。
如使用的是碱管,左手无名指及小手指夹住出口管,拇指与食指在玻璃珠所在部位往一旁(左右均可)捏乳胶管,使溶液从玻璃珠旁空隙处流出。注意:①不要用力捏玻璃珠,也不能使玻璃珠上下移动;②不要捏到玻璃珠下部的乳胶管;③停止滴定时,应先松开拇指和食指,最后再松开无名指和小指。
无论使用哪种滴定管,都必须掌握下面三种加液方法:①逐滴连续滴加;②只加一滴;③使液滴悬而未落,即加半滴。
滴定操作中应注意以下几点:
⑴ 摇瓶时,应使溶液向同一方向作圆周运动(左右旋转均可),但勿使瓶口接触滴定管,溶液也不得溅出。
⑵ 滴定时,左手不能离开活塞任其自流。
⑶ 注意观察溶液落点周围溶液颜色的变化。
⑷ 开始时,应边摇边滴,滴定速度可稍快,但不能流成“水线”。接近终点时,应改为加一滴,摇几下。最后,每加半滴溶液就摇动锥形瓶,直至溶液出现明显的颜色变化。加半滴溶液的方法如下:微微转动活塞,使溶液悬挂在出口管嘴上,形成半滴,用锥形瓶内壁将其沾落,再用洗瓶以少量蒸馏水吹洗瓶壁。用碱管滴加半滴溶液时,应先松开拇指和食指,将悬挂的半滴溶液沾在锥形瓶内壁上,再放开无名指与小指。这样可以避免出口管尖出现气泡,使读数造成误差。
⑸ 每次滴定最好都从0.00开始(或从零附近的某一固定刻度线开始),这样可以减小误差。
(6)滴定结束后,滴定管内剩余的溶液应弃去,不得将其倒回原瓶,以免沾污整瓶操作溶液。随即洗净滴定管,并用蒸馏水充满全管,备用。
读数
装满或放出溶液后,必须等1~2分钟,使附着在内壁的溶液流下来,再进行读数。如果放出溶液的速度较慢(例如,滴定到最后阶段,每次只加半滴溶液时),等0.5~1分钟即可读数。每次读数前要检查一下管壁是否挂水珠,管尖是否有气泡。
必须读到小数点后第二位,即要求估计到0.01mL。注意,估计读数时,应该考虑到刻度线本身的宽度。
读取初读数前,应将管尖悬挂着的溶液除去。滴定至终点时应立即关闭活塞,并注意不要使滴定管中的溶液有稍许流出,否则终读数便包括流出的半滴液。因此,在读取终读数前,应注意检查出口管尖是否悬挂溶液,如有,则此次读数不能取用。