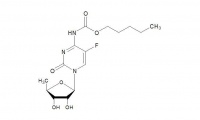
卡培他滨
英文名称:Capecitabine
化学名:5'-脱氧-5-氟-N-[(戊氧基)羰基]胞啶
分子式:C15H22O6N3F
Cas No:154361-50-9
分子量:359.35
干燥失重:≤1.0%
含 量:大于99.0%
有关物质:<0.5%
药理作用
Classification: Antineoplastic, antimetabolite
Action/Kinetics: An oral prodrug of 5'-deoxy-5-fluorouridine (5'DFUR) that is converted to 5-fluorouracil (5-FU). 5-FU is metabolized to 5-fluoro-2-deoxyuridine monophosphate (FdUMP) and 5-fluorouridine triphosphate (FUTP) which cause cell injury in two ways. First, FdUMP and the folate cofactor, N5-10-methylenetetrahydrofolate, bind to thymidylate synthase to form a covalently bound ternary complex which inhibits the formation of thymidylate from uracil. Thymidylate is essential for the synthesis of DNA so a deficiency inhibits cell division. Secondly, nuclear transcriptional enzymes can mistakenly incorporate FUTP in place of uridine triphosphate during RNA synthesis; this interferes with RNA processing and protein synthesis. Readily absorbed from the GI tract. Peak blood levels, capecitabine: 1.5 hr; peak blood levels, 5-FU: 2 hr. Food reduces the rate and extent of absorption. t1/2, capecitabine and 5-FU: 45 min. Metabolites excreted in the urine.
适应症
希罗达适用于紫杉醇和包括有蒽环类抗生素化疗方案治疗无效的晚期原发性或转移性乳腺癌的进一步治疗。
Metastatic breast cancer in those resistant to both paclitaxel and an anthracycline-containing chemotherapy regimen or resistant to paclitaxel and for whom further anthracycline therapy is not indicated (e.g., those who have received cumulative doses of 400 mg/m2 of doxorubicin or doxorubicin equivalents).
用法用量
每日,500mg/m2,连用两周,休息一周。每日总剂量分早晚两次于饭后半小时用水吞服。如病情继续恶化或产生不能耐受的毒性时应停止治疗。
Tablets Metastatic breast cancer. 2,500 mg/m2/day in two divided doses about 12 hr apart at the end of a meal for 2 weeks. Follow by a 1-week rest period (i.e., 3-week cycles).
希罗达所引起的毒性有时需要做对症处理或对剂量进行调整(停药或减量)。一旦减量,以后不能再增加剂量。
以下是对毒性进行剂量调整时的推荐剂量(根据加拿大国家癌症研究所制定的常见毒性标准)。
1级、2级:
第一次出现:停止治疗,直到恢复至0-1级水平时,按维持剂量的100%进行下一疗程治疗。
第二次出现:停止治疗,直到恢复至0-1级水平时,按维持剂量的75%进行下一疗程治疗。
第三次出现:停止治疗,直到恢复至0-1级水平时,按维持剂量的50%进行下一疗程治疗。
第四次出现:永久停止治疗。
3级:
第一次出现:停止治疗,直到恢复至0-1级水平时,按维持剂量的75%进行下一疗程治疗。
第二次出现:停止治疗,直到恢复至0-1级水平时,按维持剂量的50%进行下一疗程治疗。
第三次出现:永久停止治疗。
4级:
永久停止治疗。
如停药后需继续治疗,则应考虑到病人的最大益处,且在毒性症状恢复至0-1级水平时以推荐剂量的50%进行使用。
特殊人群的剂量调整
对肝转移引起的轻度至中度肝功能不全的病人所进行的希罗达药代动力学研究表明,无需对这类病人做剂量调整。
儿童:
尚未在儿童中进行希罗达的疗效与安全性研究。老年人:无须作剂量调整。但在老年人(65岁以上)比年轻人更易对卡培他滨产生毒性,故应对其进行密切监测。
禁 忌 症
有希罗达严重副反应或对氟脲嘧啶(卡培他滨的代谢产物)有过敏史者禁用。
注意事项
Pregnancy Category: D
Contraindications: Lactation.
Special Concerns: Use with caution in impaired renal function and in the elderly. Those over 80 years may experience a greater incidence of GI side effects. Safety and efficacy in children less than 18 years of age have not been determined. Use caution not to confuse Xeloda (capecitabine) with Xenical (orlistat).
不良反应
GI: Diarrhea (may be severe), N&V, stomatitis, abdominal pain, constipation, dyspepsia, intestinal obstruction, rectal bleeding, GI hemorrhage esophagitis, gastritis, colitis, duodenitis, haematemesis, necrotizing enterocolitis oral/ GI/esophageal candidiasis, gastroenteritis. CV: Cardiotoxicity (MI angina, dysrhythmias, ECG changes, cardiogenic shock, sudden death ), angina pectoris, cardiomyopathy hypotension, hypertension, venous phlebitis, thrombophlebitis, DVT, lymphedema, pulmonary embolism, CVA. Hematologic: Neutropenia (grade 3 or 4), thrombocytopenia, decreased hemoglobin, anemia, lymphopenia, coagulation disorder, idiopathic thrombocytopenia, pancytopenia, sepsis. Dermatologic: Hand-and-foot syndrome, dermatitis, nail disorder, increased sweating, photosensitivity, radiation recall syndrome. Neurological: Paresthesia, fatigue, headache, dizziness, insomnia. CNS: Ataxia, encephalopathy, decreased level of consciousness, loss of consciousness, confusion. Metabolic: Anorexia, dehydration, cachexia, hypertriglyceridemia. Respiratory: Dyspnea, epistaxis, bronchospasm, respiratory distress, URTI, bronchitis, pneumonia, bronchopneumonia, laryngitis. Musculoskeletal: Myalgia, pain in limb, bone pain, joint stiffness. GU: Nocturia, UTI. Hepatic: Hepatic fibrosis, cholestatic hepatitis, hepatitis. Miscellaneous: Hyperbilirubinemia (grade 3 or 4), eye irritation, pyrexia, edema, chest pain, drug hypersensitivity.
相互作用
Antacids / ↑ Absorption of capecitabine Coumarin derivatives (warfarin) / ↑ Risk of bleeding and altered coagulation test results Leucovorin / ↑ 5-FU levels → ↑ toxicity; deaths from severe enterocolitis, diarrhea, and dehydration seen in elderly clients receiving both drugs
药物过量
Symptoms: N&V, diarrhea, GI irritation and bleeding, bone marrow suppression. Treatment: Supportive medical interventions, dose interruption, adjust dose.
预防措施
需限制剂量的毒性包括:腹泻、腹痛、恶心、胃炎及手足综合征。近半数接受希罗达治疗者会诱发腹泻,对发生脱水的严重腹泻者应严密监测并给予补液治疗。每日腹泻4-6次或者夜间腹泻者为2级腹泻,每日腹泻7-9次或大便失禁和吸收障碍者为3级腹泻,每日腹泻10次以上或有肉眼血便和需静脉补液者为4级腹泻。如发生2、3或4级腹泻,则应停用希罗达,直到腹泻停止或腹泻次数减少到1级时再恢复使用。3级或4级腹泻后再使用希罗达应减少用量。几乎近一半使用希罗达的病人发生手足综合征,但多为1-2级,3级综合征者不多见。多数副反应可以消失,尽管需要暂时停止用药或减少用量,但无须长期停止治疗。
妊娠及哺乳妇女
尚未在妊娠妇女中进行希罗达临床研究,但必须要考虑到如果在这类病人中使用希罗达,可能会引起胎儿损伤。动物实验表明卡培他滨能导致胎儿死亡或畸形。这些发现预示卡培他滨衍生物也具有这种作用,因此不能在妊娠妇女中使用希罗达。如在妊娠期间使用希罗达,或在使用希罗达期间发生妊娠时,必须考虑到该药对胎儿损伤或致畸的潜在危险性。生育期妇女使用希罗达时必须采取避孕措施。
尽管尚不知希罗达是否能分泌于奶液中,但由于许多药物能在奶液中分泌而有对哺乳的婴儿造成严重副反应的潜在危险性,因此建议使用希罗达的妇女停止授乳。
副 反 应
希罗达的副反应较少,以下情况可能与之有关:
消化系统:希罗达最常见的副反应为可逆性胃肠道反应,如腹泻、恶心、呕吐、腹痛、胃炎等。
严重的(3-4级)副反应相对少见。
皮肤:在几乎一半使用希罗达的病人中发生手足综合征:表现为麻木、感觉迟钝、感觉异常、麻刺感、无痛感或疼痛感,皮肤肿胀或红斑,脱屑、水泡或严重的疼痛。皮炎和脱发较常见,但严重者很少见。
一般不良反应:常有疲乏但严重者极少见。其他常见的副反应为粘膜炎、发热、虚弱、嗜睡等,但均不严重。
神经系统:头痛、感觉异常、味觉障碍、眩晕、失眠等较常见,但严重者少见。
心血管系统:下肢水肿较轻且不常见。尚未见其他心血管系统副作用。
血液系统:中性粒细胞减少且少见也不严重,贫血极少见也不严重。
其他:厌食及脱水常见,但重者极少见。
联合用药
希罗达与大量药物合用,如抗组胺药,NSAIDs,吗啡,扑热息痛,阿斯匹林,止吐药,H2受体拮抗剂等,未见具有临床意义的副作用。
蛋白结合:卡培他滨与血清蛋白结合率较低(64%)通过置换与能蛋白紧密结合的药物发生相互作用的可能性尚无法预测。
与细胞色素P450酶间的相互作用:在体外实验中,未发现卡培他滨对人类肝微粒体P450酶产生影响。
药物过量
希罗达的临床试验中,未发现由于药物过量而引起的副反应。但动物实验(对猴类以25,679mg/m2/天的积极治疗)以及对人以最大耐受剂量(3,514mg/m2/天)治疗中,药物过量的表现为恶心、呕吐、腹泻、胃肠激惹、肠胃出血和骨髓抑制等。处理方法应包括使用利尿剂脱水治疗,必要时透析治疗。
规 格
0.5g*30片/盒。
批准文号
国药准字J20030108。
生产企业
瑞士巴塞尔豪夫迈.罗氏有限公司制造(上海罗氏制药有限公司分装)。
参看
| ||||||||